言わずもがなの議論だが、ついでにもう一つ、はなはだ危険な爆弾を投げてみよう。若者は、この仮説を決して鵜呑みにしないで欲しい。この「極々少数派の仮説」を試験の解答として書いた場合、試験に通るかどうか保証はできない。近頃、自分が教えたことから外れた解答を書くと、内容を吟味することなく怒って単位を出さない小物教授がいるからである。いや、昔もいたか!しばらくは正統派の理論に従っていた方が無難である。では、危険な「極々少数派の仮説」とはどんなものであるか。
さて、まずアブシジン酸の定義から話を始めたい。ちょっとだけ日本語のサイトを回ってみたが、どこも「アブシジン酸は植物ホルモンである」ということを前提にして、その生理活性を説明するという形になっている。いくつかの、植物生理学分野における代表的書籍においても、これは変わらない。「アブシジン酸は植物ホルモンである」と書いてあると我々はどう受け取るのだろう。
素直な私は、「うむ、アブシジン酸はホルモンか。ホルモンは非常に生理活性の高い化合物である。きっと、生体内での濃度は厳密に制御されているに違いない。つまり、生合成系と生分解(不活性化を含む代謝系)が、完全に構築され精緻に制御されているだろう。ストレスがかかれば速やかに生合成が行われ、ストレスが解除されると速やかに代謝され活性を失うに違いない」と考える。ここまでの考えは、多くの方々と大きく乖離することはないと思う。
話は少し変わるようだが、植物の中でゲノムの解析がすすめられ、シロイヌナズナ(Arabidopsis thaliana )をはじめとして30種弱の植物の全塩基配列が得られている。(ドラフト配列を含む)ここでは、KEGGにおいて利用可能な形になっている以下の26種の植物を使って議論しよう。
Plants (26)
Eudicots (11) 真正双子葉植物
Mustard family (2) アブラナ科
ath Arabidopsis thaliana (thale cress) シロイヌナズナ
aly Arabidopsis lyrata (lyrate rockcress) ミヤマハタザオ
Pea family (3) マメ科
gmx Glycine max (soybean) ダイズ
mtr Medicago truncatula (barrel medic) タルウマゴヤシ
cam Cicer arietinum (chickpea) ヒヨコマメ
Rose family (1) バラ科
fve Fragaria vesca (woodland strawberry) エゾノヘビイチゴ
Cucumber family (1) ウリ科
csv Cucumis sativus (cucumber) キュウリ
Spurge family (1) トウダイグサ科
rcu Ricinus communis (castor bean) トウゴマ
Willow family (1) ヤナギ科
pop Populus trichocarpa black cottonwood
Grape family (1) ブドウ科
vvi Vitis vinifera (wine grape) ヨーロッパブドウ
Nightshade family (1) ナス科
sly Solanum lycopersicum (tomato) トマト
Monocots (6) 単子葉植物
Grass family (6) イネ科
osa Oryza sativa japonica (Japanese rice) イネ ジャポニカ
bdi Brachypodium distachyon セイヨウヤマカモジ
sbi Sorghum bicolor (sorghum) ソルガム
zma Zea mays (maize) トウモロコシ
sita Setaria italica (foxtail millet) アワ
Ferns (1) シダ植物
smo Selaginella moellendorffii イヌカタヒバ
Mosses (1) 蘚類
ppp Physcomitrella patens subsp. patens ヒメツリガネゴケ
Green algae (6) 緑藻類
cre Chlamydomonas reinhardtii クラミドモナス
vcn Volvox carteri f. nagariensis ボルボックス
olu Ostreococcus lucimarinus オステロコッカス
ota Ostreococcus tauri オステロコッカス タウリ
mis Micromonas sp . RCC299 ミクロモナス
mpp Micromonas pusilla ミクロモナス プシラ
Red algae (1) 紅藻類
cme Cyanidioschyzon merolae シアニディオシゾン
http://www.genome.jp/kegg-bin/get_htext?htext=br08601_map00906.keg&hier=5 から引用 (分類名と和名は筆者の責任で追加している。)
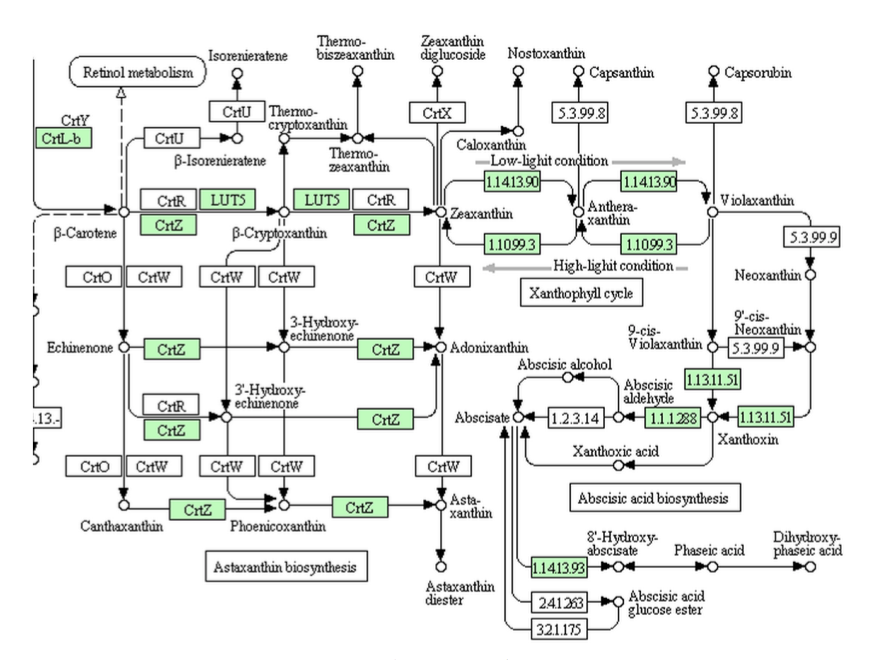
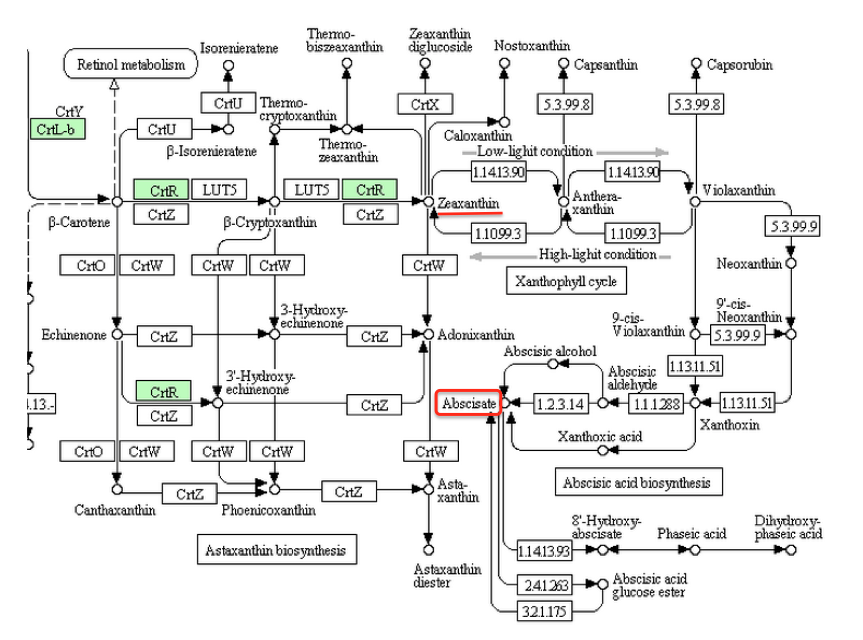
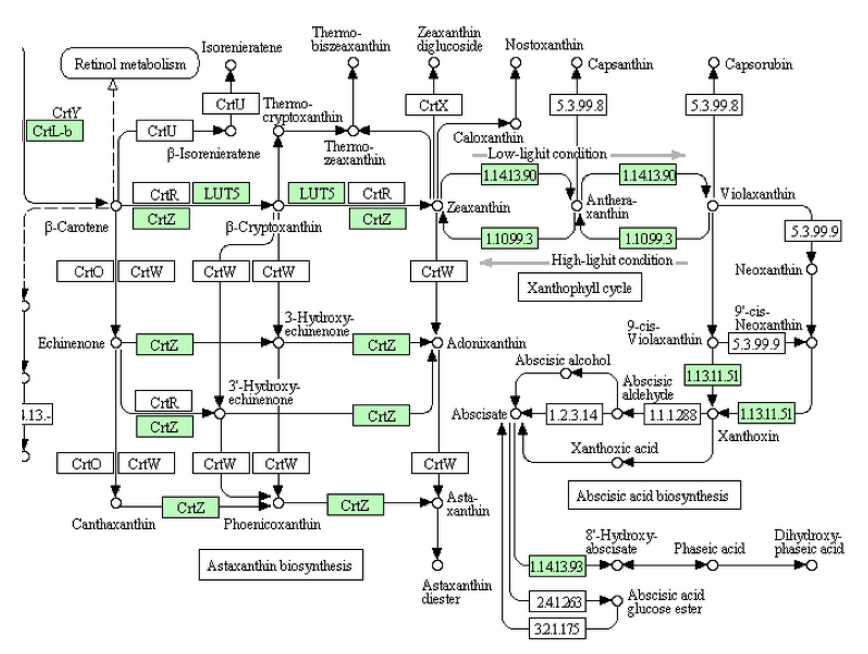
以下の議論で使う図は、すべてKEEGのカロチノイド代謝系からの引用である。こうした議論をする上で、KEEGにはいくら感謝してもし過ぎることはない。このデータベースがなければ、私は何もできなかったに違いない。そこで、まず紅藻類のシアニディオシゾン、すなわちイタリアの温泉に生育する単細胞性の藻類についての議論である。先に、紅藻にもアブシジン酸は分布すると書いた。さらに、紅藻に属するアマノリやオゴノリなどはアブシジン酸を含み、このアブシジン酸が生育阻害活性を持つ、そして紅藻に由来するアピコプラストをもつトキソプラズマにおいては、アピコプラストにおいてアブシジン酸が生産されるとも書いた。ところが下図を見て欲しい。
紅藻類であるシアニディオシゾンのアブシジン酸生合成系?
紅藻類であるシアニディオシゾンの代謝系を見ると、アブシジン酸どころかゼアキサンチンまでで生合成は止まっている。(枠内が緑色にぬってある酵素が、この生物に存在する酵素である。以下の図においても同じ)困ったことだが、2021年段階のKEGGにおいてはβ-カロテンで生合成系は止まっているようになっているのである。まあ、シアニディオシゾンは原始的紅藻であって、もう少し進化した紅藻はアブシジン酸を生合成できるのではないかと考えたいところだが、どうもそういうことにはならなさそうな気がする。理由は以下に述べる。
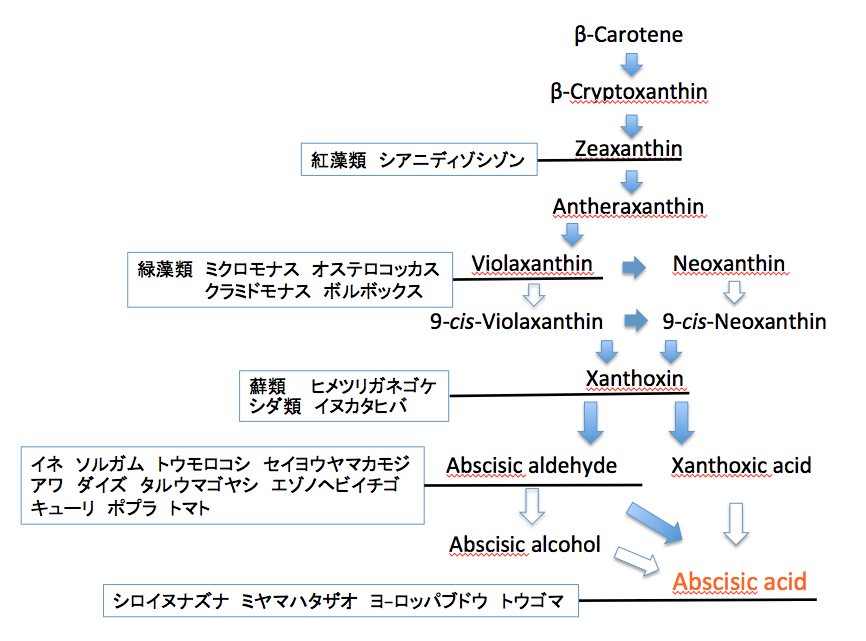
緑藻類を見てみよう。緑藻類であるHaematococcus pluvialis においては、酸化ストレスで誘導されるアブシジン酸が耐乾燥性をもつシストへの形態変化を誘導したり、クラミドモナス(Chlamydomonas reinhardtii )においてカタラーゼやアスコルビン酸ペルオキシダーゼを誘導して酸化ストレス抵抗性を向上させるという報告がある。では、ゲノム解析の終わった6種の緑藻について、生合成系がどこまで伸びているか、順に示していく。
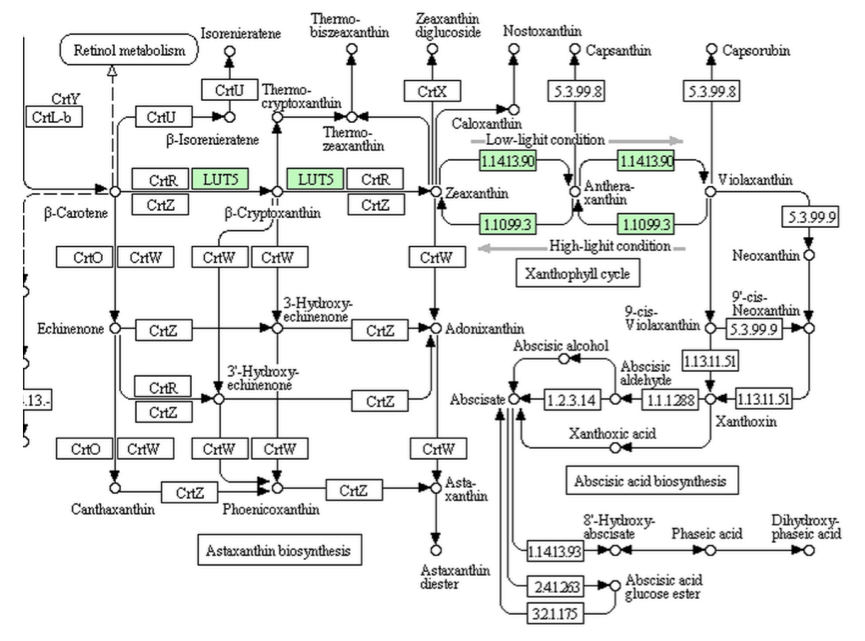
ミクロモナス(緑藻類)のアブシジン酸生合成系?
Micromonas においては上に示すように、ビオラキサンチンまでの生合成酵素はあるが、それ以降の反応を触媒する酵素は存在しない。原始的な緑藻と言われているOstreococcus においても同様である。この2種においては、リコペンからγ-カロテンを通ってβ-カロテンへ導く酵素もないことになっている。では、クラミドモナスにおいてはどうなっているのか?下に、クラミドモナスとボルボックスの持つ経路を示す。
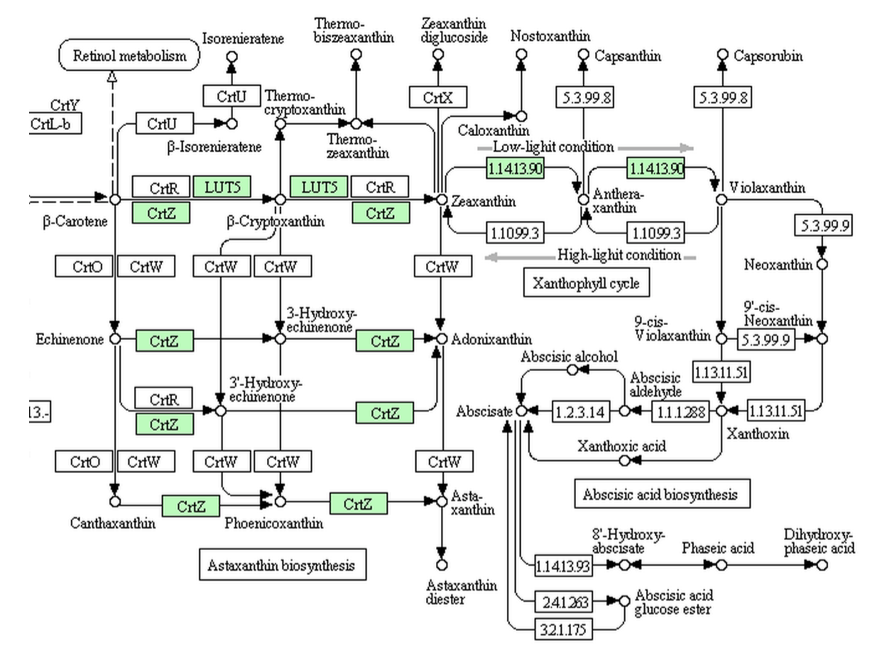
クラミドモナス(緑藻類)のアブシジン酸生合成系
困ったことなのだが、クラミドモナスとボルボックスもアブシジン酸まで達する経路は持たず、ビオラキサンチンでアブシジン酸生合成系は途絶えている。つまりここにおいても、アブシジン酸の生合成系も分解系であるファゼイン酸生合成系も存在しないにもかかわらず、アブシジン酸が働いているということになる。
蘚類においてはヒメツリガネゴケのゲノム解析が終わっている。「アブシジン酸は蘚類以上の高等植物に分布し・・・」と書かれているので、ここでは合理的な結果が得られることを期待して、KEGGにアクセスすると、次の図が得られた。
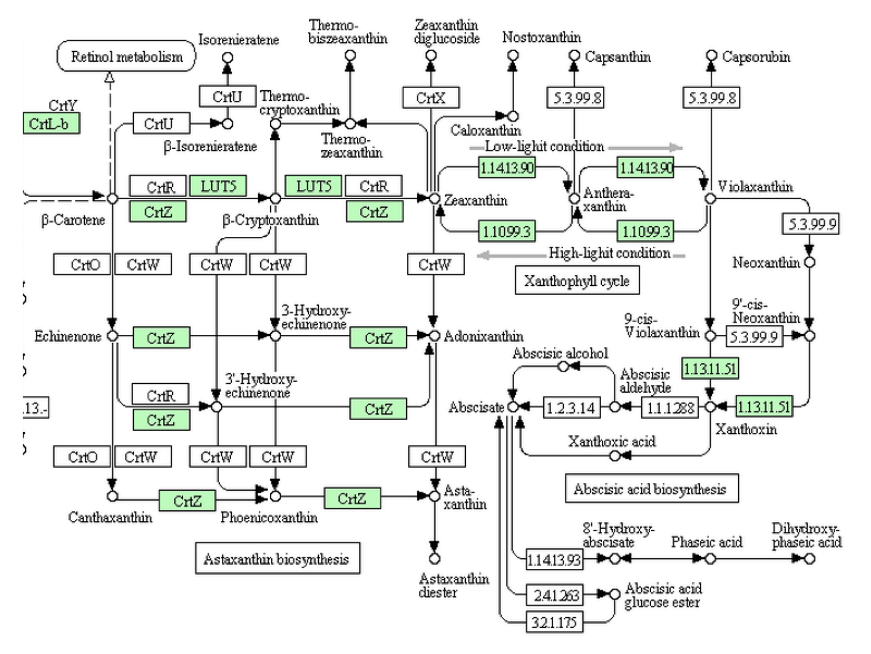
ヒメツリガネゴケ(蘚類)のアブシジン酸生合成系
アブシジン酸へ向かう生合成系は、緑藻類ではビオラキサンチンまでしか伸びていなかったが、ヒメツリガネゴケでは一歩進んでXanthoxinまで伸びている。しかし、Xanthoxinから先の生合成を担う酵素は未だ知られていない。いやいや、ヒメツリガネゴケはコケコケ、下等なコケだよ。研究の進んでいないそんな下等なコケではなく、シダ類以上であれば、調った生合成と生分解系の姿が見られるに違いない。
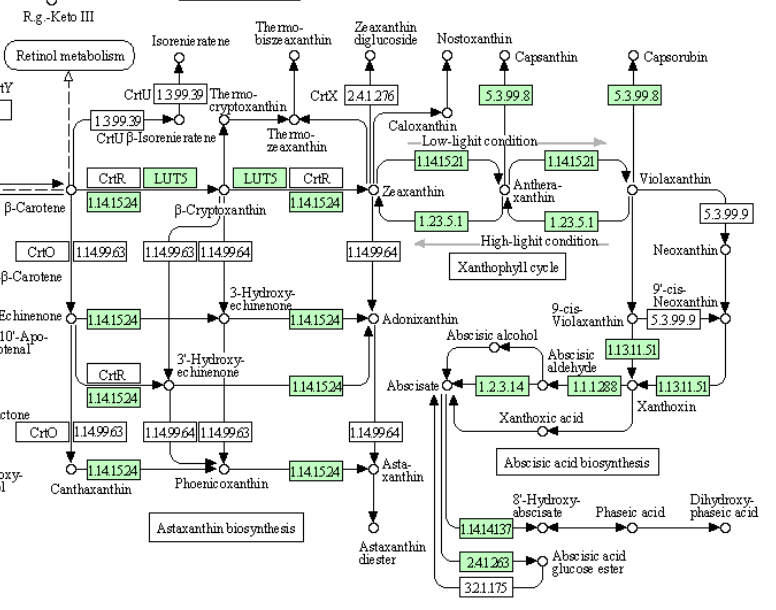
イヌカタヒバ(シダ類)のアブシジン酸へ向かう生合成系
シダ類においてゲノム解析の終わっている植物はイヌカタヒバ(Selaginella moellendorffii )、ヒカゲノカズラ植物門イワヒバ科に属するシダ植物で、日本にも広く分布する。この植物においては、問題なく調った生合成と生分解系の姿が見られるのか。上図をみて欲しいのだが、生合成酵素についてヒメツリガネゴケと同じくXanthoxinまでの酵素を持つのだが、XanthoxinからAbscisic aldehyde をつなぐ酵素は持たない。にもかかわらず、2021年段階のKEEGに置いてはAbscisic aldehyde を酸化してアブシジン酸を作る酵素(1.2.3.14)は存在するし、アブシジン酸を不活性化して8’-ヒドロキシアブシジン酸に導く酸素添加酵素も存在する。いやいやいや、アブシジン酸を作る酵素がないのに酸化して不活性化する酵素はある、ちょっと矛盾するような気もしないではないが、たった1種のシダ、知識の蓄積が足りない。アブシジン酸は植物ホルモン、シダ植物を含む高等植物の植物ホルモン。研究の進んだ高等植物においてはきっと完璧だよ。完璧!!
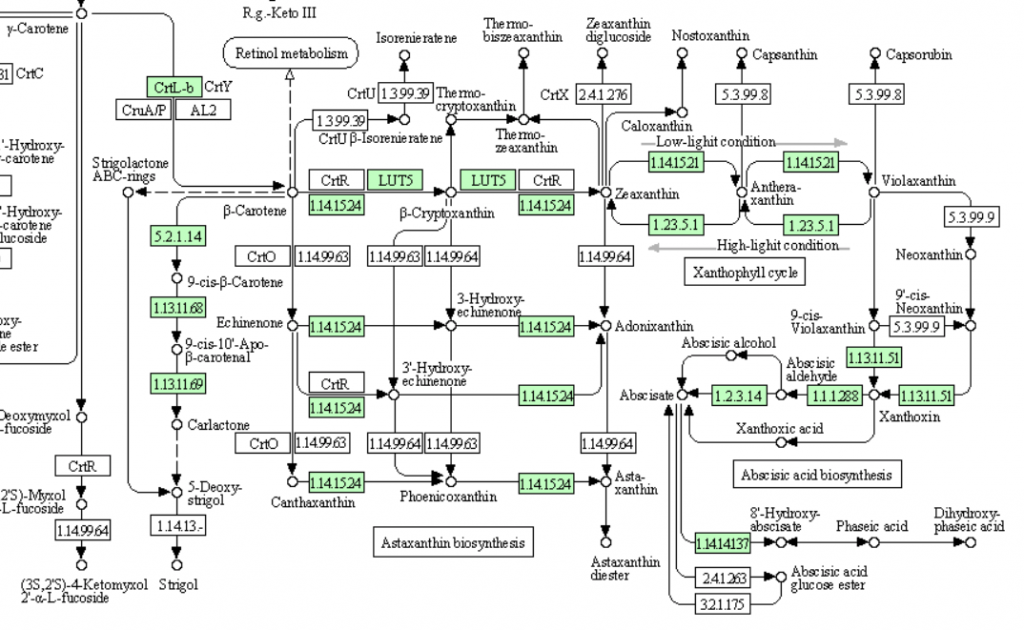
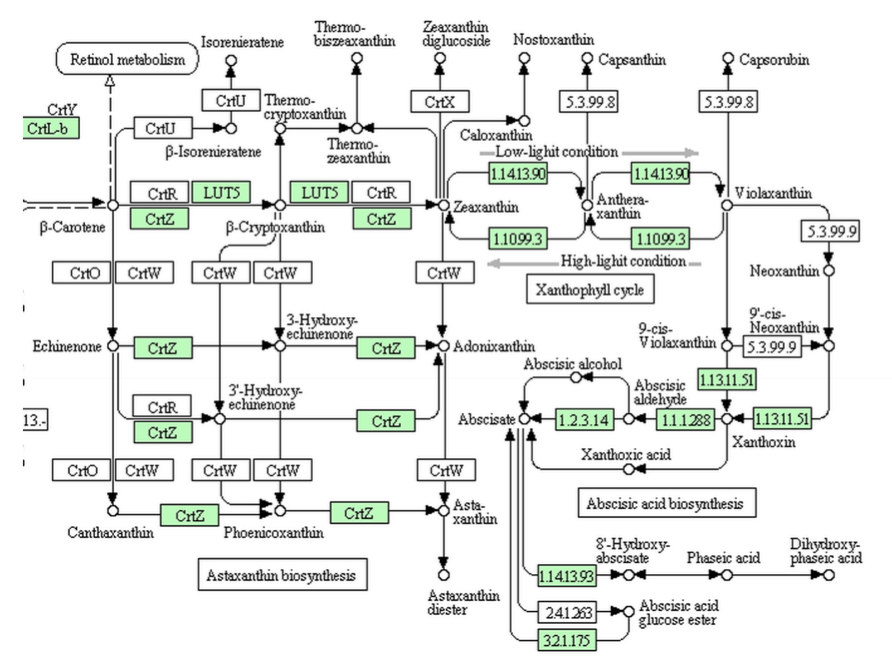
さて、高等植物なら研究の進んでいるアラビドプシス(シロイヌナズナ)、これを見るべきであろう。現代の植物学において、アラビドプシスを語らずして何をか況んや。というわけで、シロイヌナズナについてKEGGのデータをみてみると、下図のようになっている。
シロイヌナズナ(カラシナ科)のアブシジン酸の生合成経路
確かに完璧である。生合成系がきちんとアブシジン酸まで伸長しているだけでなく、濃度調節に働くかもしれない8’-ヒドロキシアブシジン酸への代謝系も揃っているではないか。ファゼイン酸への代謝とアブシジン酸のグルコースエステルを作る酵素がないのに、その分解酵素がある点は少し気になるが、ここは目を瞑って、完璧完璧!同じカラシナ科でゲノム解析の終わっているミヤマハタザオ、トウダイグサ科のトウゴマ、ブドウ科でワインの原料であるヨーロッパブドウ、何れもアラビドプシスと同じ代謝系を持っているではないか。高等と言われる植物は、こうでなくてはいけない。
とは言うものの、ここまでの代謝系が完成していない植物群のアブシジン酸生合成と生分解をどう理解すればいいのか。ある段階の反応を触媒するとされる酵素が無いにもかかわらず、生成物は生産されているという現象こそが、酵素の甘い基質特異性に由来していると考えていいのではないか。(もちろんその段階を担う酵素として特定されていない、現に2021年段階で空欄が埋まった酵素があるではないかという考えもありうる。しかし、2021年段階で以前に特定されていた酵素が外される例も存在する。困ったことである。)触媒活性自体はさほど高くないが故に、ある段階を触媒する酵素と特定できないが、その甘い基質特異性ゆえに、その段階を進めることができるいくつかの酵素群が、酵素が特定されていない反応を担保していると考えざるを得ないだろう。