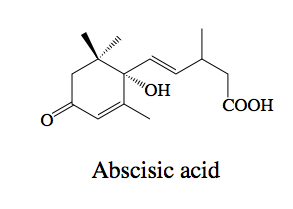
アブシジン酸について、最初に一般的な歴史を書いておくことにする。分析機器の著しい進歩に伴い、1950年頃から植物の休眠や生長を制御する微量物質についての研究が休息に進みはじめた。アブシジン酸について言えば、1961年にLiuとCarnsがワタの果皮から葉柄での離層形成を促進する物質を単離し、この物質に脱離という意味を持つabscissionに因んでabscisinと命名したとされている。1963年には、大熊が参加していたAdicottらのグループが、ワタ未熟果実から同様の活性を持つ物質を単離しabscisin Ⅱと命名した。同年、EaglesとWareing は、ヨーロッパダケカンバ (Betula pubescens) に含まれる休眠を制御する物質を単離し、休眠 dormancy に因んでdorminと命名した。一つの化合物に二つの名前がつけられたため、1967年の第6回国際植物生長物質会議 (IPGSA) において摺り合わせが行われ、abscisin Ⅱ、dorminの名称を「Abscisic acid」、略称を「ABA」と統一することが決定され現在に至っている。
アブシジン酸はいろんな意味で幾分以上にややこしい化合物である。名称からして錯綜している。我々はアブシジン酸で教えられたが、近頃正式名称がアブシシン酸に決まったと聞く。しかし、世の中にはアブサイジン酸、アブスシン酸という表記もあればアブサイシン酸という表現もある。外国語を日本語にして表記する場合、いくつかの書き方が出てくることに不思議はない。
例えば、ゲーテにギョエテ、ゲエテ、ゲョエテなど多数の表記があったことは知っているし、ローマ字表記法で有名なヘボン式のヘボンの部分が Hepburn であり、オードリー ヘップバーンのヘップバーンと同じであることも知ってはいる。オードリー ヘップバーンをオードリー ヘボンと表記していたとすれば、日本での彼女の人気は少し落ちたのではないだろうか。さて、ゲーテとヘップバーンの場合は、原語における一つの発音を、異なった発音様式を持つ日本人がどのように聞き、表記したかの問題である。しかし、アブシジン酸の場合はこの範疇を越える問題である。ネイティブがアブシジック アシッドと発音しているのを、アブサイシック アシッドと聞き取ることはないだろう。では、錯綜した名称はどれが正しいのか。
以下、私見である。アブシジン酸の名称は、殆どの場合脱離を意味するabscissionに由来すると書いてある。そうであれば、abscisic のabの部分は「離脱」「分離」を意味する接頭語であり、[æb-, əb-]という音を持つ。アブまでの発音は共通しているので、問題はscisicをどう読むかという問題になる。つたない英語力しかない私の感覚では、長年使われてきたアブシジン酸という読み方は英語としてあまりみかけない発音だと考えて、scienceから連想されるサイという発音、つまりアブサイシン酸でも良いのかななどと安易に考えていたのである。
ところが近年、化合物名字訳基準でアブシシン酸が採用されたと聞き、改めてscisicについて考え直してみた。1961年にLiuとCarnsが、Scienceに投稿した論文で使用したabscisinという名称が、1963年大熊等によるabscisin Ⅱの命名に引き継がれたのであろうことは容易に推測できる。そこでscisinというフレーズをあれこれしらべてみたが、この部分の語源となりそうなものは存在しないし、scisicを語尾に持つ適切な例も存在しない。この名称が脱離を意味するabscissionに因んで命名されたとされているため、あらためてabscissionについて辞書を引いてみると、なんとabscissionの発音は[æbsíʒən] となっている。アブシッションではなく後ろのssionの部分はアブシジャンと濁るのである。さらにabを除いたscissionも、分割、分離の意味を持つ名詞であり、その発音は[síʒən]と濁っていたのである。そういえば、高校の頃に覚えたscissorsもシザースであった。いやいや、アブシジン酸という和名をつけられた先達に、あらためて敬意を表したい。納得!!
ではそれ以外の発音は、何に由来するのか? 脱離するという意味を持つabsciseという自動詞がある。同じく切り離すという意味を持つabscindという他動詞が存在する。前者の発音はəbˈsaɪzまたはæbˈsaɪzであり、後者の発音はəbˈsɪnd, æbˈsɪndである。これらの場合、sciの部分はsaiあるいはsiと発音する。LiuとCarnsが、脱離するという意味を持つ自動詞 absciseを語源としてabscisinとしたのであれば、abcsicinの発音はアブサイシンが妥当であろう。abscindを語源とするのは一寸考えにくいが、もしそうならアブシシンも正当性を持つのかもしれない。
彼らがabscissinと表記していたならば、間違いなくアブシジンであり、abscissic acid であれば間違いなくアブシジン酸となりこんな混乱は起こらなかったであろう。しかし、現実の化合物名はabscisinであり、sが1文字省いてある。abscisic acidという化合物名は、この1つのsを除いたabscisin、abscisinⅡを語源にすると同時に、この化合物がカルボン酸であることを考慮して作られたのであろう。ちなみに、abscisinの名付け親であるLiuとCarnsの二人は、abscisinをどう発音していたのだろう。アブシジン酸で教育を受けた私は、かすかな違和感を感じながらもアブシシン酸なる用語を使わないといけないのであろうか。
さて、私が1970年頃に農薬化学という講義の中で植物ホルモンとして教えられたのは、オーキシン(インドール酢酸)、サイトカイニン(ゼアチン)、ジベレリン(ジベレリン酸)、アブシジン酸、そしてエチレンの5種類の化合物であった。
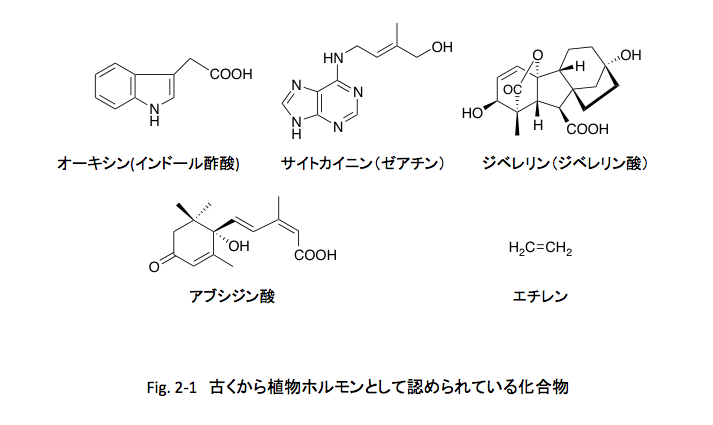

この5種類の化合物、図2-1にその構造式を示しているが、構造式を眺めても生合成を考えても、どうにも収まりが悪い。収まりが悪いと云う感覚は有機化学と生合成を基盤に考えていた個人的な感覚であって、周りの人々がどう感じていたかについては分からない。動物で主要な働きをしているステロイドホルモンやペプチド性ホルモンなどに対応するものがないことも不可解だった。とにかく5種のホルモン分子について、それら分子が位置する生合成的カテゴリーとヒエラルキーのアンバランスさに納得がいかなかったわけである。
生合成的カテゴリーとヒエラルキーのアンバランスに対する違和感といっても、それはおまえの感じ方に過ぎないといわれれば、確かにそうである。しかし、オーキシンいわゆるインドール酢酸は、どう見てもアミノ酸であるトリプトファンと関係を持った化合物である。サイトカイニンは核酸塩基と同じくプリン環を持つ化合物で、生合成的にみるとtRNA(運搬RNA)に由来する経路と、ATPまたはADPがイソペンテニル化された後、リン酸、リボースが脱離する経路で生合成されるという。ジベレリンとアブシジン酸はテルペンに属するが、前者は4個のイソプレンユニットが結合したゲラニルゲラニル-ジリン酸から誘導される3環性ジテルペン酸であるのに対し、後者にはC15のファルネシルピロリン酸から直接環化する経路と、C40のβ-カロテンを通り、環の酸化と炭素鎖の酸化解裂によってつくられる二つの経路が存在するという。エチレンについては気体の炭化水素で、最も簡単なアルケンである。エチレンに特異的なレセプターなど、何となく考えにくいと思っていた。なぜそんな分子がホルモンであるのかという問いに対しては、それらが微量で合目的的活性を持つではないかという答えが返ってきた。ほとんど何も分かっていなかった私としては、ホルモンの定義を適用すればそうなるけれどと、不満げに認めるしかなかった。
このもやもやとした疑問は植物ホルモンに対してだけ感じていたわけではない。動物のホルモンに対しても同種の違和感があった。いわゆる低分子の化合物(ステロイド、チロキシン、アドレナリンなど)とペプチド性化合物を、どうしてホルモンという単一の概念で括る事ができるのだろうか。いわゆるホルモンという古典的な定義を適用すればそうなるのだが、個々の化合物のあまりの違いが納得を阻害した。喉をこするようなこの違和感が、以下の話の下敷きになっていることは間違いない。
オーキシンの発見以後、植物にはオーキシンの活性を抑制するだけでなく、休眠や脱離を誘導する物質があることが知られていた。カリフォルニア大学のLiuとCarnsが、1961年にワタ葉柄の離層形成促進物質を単離しabscicinと命名した。だが、ここにも問題がある。Wikipedia には「ワタの葉柄から単離した落葉促進物質をabscission(葉などの離脱)にちなみ「アブシシン (abscisin)」と命名した」と書いてある。植物ホルモンについて言及している多くの書籍においてもほぼ同じ説明がなされている場合が多い。Wikipedia の記事はそれらからの引用であろう事は容易に推察できる。しかし、Scienceに載った原報は“A crystalline substance, which accelerates abscission of excised debladed petioles at 10-2 microgram per abscission zone, has been isolated from cotton burs. “となっている。burについていくら英和辞典を引いてみても、「いが、とげ、種や果実の外皮」という訳しかない。従って、彼らが単離したabscisinはワタの種皮からであり、切断したワタ葉柄への0.01 mgの投与によって、葉柄の離層形成を促進する効果を持つ物質だったのである。ちょっとした勘違いであろう。
繰り返しになるが、この物質を追いかけていたのは彼らだけではなく、ヨーロッパダケカンバの休眠物質を追いかけていたWareingのグループ、キバナルピナスの花の脱離物質を追いかけていたvan Steveninckのグループ、ワタ幼果の落果促進物質を追いかけていたAddicottのグループなどである。この中で構造決定に至ったのは、日本人を含むOhkuma, K., Lyon, J. L., Addicott, F. T., Smith, O. E. のグループと、サイカモアカエデから単離したDorminの構造を決めたCornforth, J. W. Milborrow, B. V. Ryback, G.and Wareing, P. F. のグループであった。
前者は、構造を決めた物質にLiuとCarnsのabscisinを考慮してAbscicin Ⅱと命名している。後者は、休眠を意味するdormancyに因んだDorminという名称を与えている。1965年に両グループが同じ構造式を提出したため、当然先陣争いが起こったのであろう。この間の事情についてはよく分からないし、首を突っ込む必要はないが、 アブシジン酸構造の prior claim(先取特権)について、何らかの争いめいたことがあったようだ。http://plantphys.info/plant_physiology/dormin.shtmlのサイトには、かなり厳しい書き込みがされている。ともあれ、1968年の国際植物生長物質会議において名称のすりあわせが行われ、この化合物をAbscisic acid (ABA) と呼ぶことが決定されたわけである。
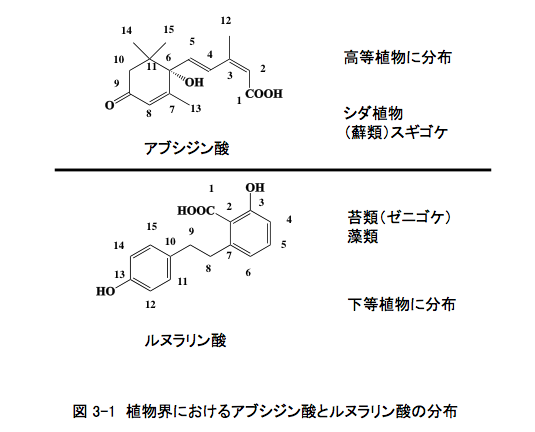
その後、この化合物については精力的な研究が行われ、蘚類(スギゴケの仲間)以上の高等植物に普遍的に含まれること、植物にストレスがかかったとき生合成され、生長の一時停止のシグナルであること、植物の休眠を制御し、水ストレスがかかったとき気孔を閉め蒸散を抑制するなど、微量で多くの合目的的作用を持つことから、5番目の植物ホルモンとして認知された。しかしながら、ABA単離の際の指標となりかつ命名の基礎となった脱離誘導が、後にABAではなく主としてエチレンによって制御されていることを考えれば、Dorminの方が好ましい命名であったような気がしないでもない。
こうして社会的に認知されたアブシジン酸については、ケモタクソノミー(含有される化学成分に基づく分類)を意識した植物界での分布、生合成のルートと制御、生分解のメカニズム、他の植物生長ホルモンとの拮抗作用を含む生理作用、農業への利用などを念頭に置いた類似物質の合成と構造活性相関など、多くの研究が進行中であった。私の考えるべき問題は、この競争に私が参加する場合どのような立場から関与すれば意義のある仕事になるかという点にあった。
当時、私が勤めていた大学には大学院はまだ設置されておらず、女性の助手1人と毎年研究室に入ってくる4〜5人の4年生だけが戦力である。微量分析を行うには、機器はもとより私の経験がなさ過ぎて、間違うリスクが大きすぎた。4年生の卒業研究としては、多段階の合成はちょっと厳しい。グレードの低いIRとUV、そして理事長を半分だまして購入した60 MHzのNMR装置では、何をすべきか考え込まざるを得ない状況だった。
「ちょっと待てというシグナルとしてのホルモン」という点に親近感を感じただけで、安易に研究課題を決めたことをほんの少し後悔した。しかし、別のテーマを立てたにしても状況が変わるわけではない。当たり前の結論であるが、結論は一つ、他のグループと同じ土俵に立ってはいけない。人と違う切り口切り口を見つけ研究を行う、それが自明の結論である。そうする以外に道がないとすれば、そうする以外に仕方がない。腰を据えて報告を読みあさった。
そして気づいたのは、すべての研究者が何の疑いもなくアブシジン酸を植物ホルモンとして認め、より精密な分析と有効利用を志向しているということである。なんと馬鹿なことに気付くのかと自嘲に近い気分になったことを記憶している。しかし、十数年前はただの脱離促進物質であり、休眠誘導物質でしかなかったアブシジン酸が、今では植物ホルモンとして認知され、合目的的活性以外は持つはずがないという前提のもとに研究されている。誰か、「この前提を疑う人はいないのだろうか?」と思ったが、そんな馬鹿なことを考える人は私しかいなかったらしい。
ここで持ち前の悪い癖が出てしまった。「なぜ、アブシジン酸は植物ホルモンであるのか?」と、改めて考えてしまったのである。なぜ、すべての研究者は、アブシジン酸が植物のホルモンであることに同意したのか? これは植物ホルモンとは何であるかという定義の問題をも含んでいる。そこで改めて植物ホルモンの定義を見直したのだが、植物ホルモンには明確な定義がされておらず、動物ホルモンの定義を少し改変して準用した形になっていた。(いまでも状況はほとんど変わっていない)
さて、動物生理学におけるホルモンは、「特定の分泌線で生合成され、血液やリンパ液で標的臓器に運ばれ、標的臓器で特異的な生理過程に影響を与える微量物質」と定義されている。ところが植物では臓器の分化が明確でないため、生合成部位・作用部位ともに特定できないことが多い。さらに内分泌という項目も血液やリンパ液による輸送という項目も成立しない。従って、このあたりの条件を緩和して、「植物に広く分布し、植物体内で生合成され、植物の特異的な生理過程を調節する微量物質」ということで大方の合意が得られているようである。アブシジン酸は、広く植物に分布し、植物体内で生合成され、低濃度で合目的的かつ特異的に働く。先の合意に従えば、確かにアブシジン酸は植物ホルモンであると判断して良いのかもしれない。
周りの研究者に「何故アブシジン酸はなぜ植物ホルモンか」と尋ねると、一瞬怪訝な顔をした後「広く植物に分布し、植物体内で生合成され、低濃度で合目的的かつ特異的に働く」ではないかという定型的な答えが返ってきた。その合意を無邪気に認めて研究を始めればいいのだが、この厄介な性格ではそれはなかなか難しい。すぐに話を大きく広げるくせに、やけに細かいところにこだわってしまう。本人が納得するまで放っておくしかないと、当の本人が考えているのである。
さて、物事を論理的に考える場合、まず考える基礎を確かなものにしておく必要がある。この場合、動物ホルモンを基礎にして植物ホルモンを定義をしているため、動物ホルモンの定義は確実なものでなければならない。ところが、当時の動物ホルモン関連分野においては、サイトカイン、オータコイド、神経伝達物質など数多くのホルモン様物質の発見が続いており、動物ホルモンの位置づけ自体が揺らぎ始めていたのである。その揺らいでいる動物ホルモンの定義から、産生臓器と輸送と標的臓器の縛りをなくしたとき、何が残るか。分布の項を除けば、植物体内で生合成され合目的的に働く微量生理活性物質といっているに過ぎない。
さらに、問題は残る。「植物に広く分布し」というフレーズの中には、異なった植物でも共通の作用を示すという暗黙の合意があるように思えるが、事はそう簡単ではない。一般的な理解において、ホルモンの持つ特異的な作用は生物間で共通であるという思い込みがあるようだ。しかし、この認識は動物ホルモンにおいてすでに崩れてしまっている。例えばチロキシン、カエルでは変態を促し、サケ科の魚においては海水への適応に働き、鳥類では換羽を誘導し、ヒトにおいては甲状腺ホルモンとして全身の細胞の代謝率を制御する。また例えばプロラクチン、淡水魚類・両生類においては浸透圧調節に働き、ハトでは素嚢上皮の増殖肥大を起こしクロップミルク(素嚢乳)分泌に働く。哺乳類では他のいくつかのホルモンと協調して、乳腺の発育を促し乳汁の分泌を引き起こす。さらにプロラクチンは爬虫類で食欲を増大させ、脂肪の蓄積を促す。そしてさらに、 プロラクチンは鳥類の渡りをも引き起こすという。動物の範囲を広げると、話はもっと変になる。昆虫の変態ホルモン(脱皮ホルモン)であるエクダイソンは、近縁である甲殻類であるエビやカニでは脱皮を促すにしても、これをヒトに与えたらどうなるか。脱皮を起こすはずはないし、変態になるのだろうか??
我々は、アプリオリにホルモンという化合物群があり、これらが動物に、植物に、あるいは微生物において同種の特異的作用を持つと無意識に錯覚してきたようだ。しかしながら、動物ホルモン、植物ホルモンに限らず、ある種の化合物群がアプリオリにホルモンとしてあるのではない。ある生物が、ある化合物を特異的生理活性物質として選択し利用しているのである。主体は生物側にあるのである。
植物ホルモンに関する研究を始めようと植物ホルモンについて考え始めたら、まずホルモンとは何かという段階でつまずいてしまった。これでは研究など進むはずはないし、この種の疑問はなかなか人に相談することもできない。仕方なく、代謝マップをただ睨めながらあれこれと考える日が続いた。「下手の考え休むに似たり」とは言うものの、やはり考えるものである。ちょっと興味深い事実に気が付いた。話を進めるために、植物ホルモン、動物ホルモンという用語にはいろいろな問題があると私は思うが、しばらくの間はこれらの用語を一般的に使われている形で使用する。
まず、動物のホルモンはステロイド類、チロキシン類、アドレナリン(エピネフリン)及びメラトニンのグループを除けば、大部分がペプチドあるいはタンパク質であるのに対し、植物のホルモンではオーキシン、ジベレリン、サイトカイニン、アブシジン酸、エチレンのすべてが低分子の有機化合物である。その頃、植物ホルモン候補に挙がっていたブラシノステロイドあるいは植物ホルモン候補と言われている、ジャスモン酸、サリチル酸、ストリゴラクトン、ポリアミンあるいは一酸化窒素も例外ではない。
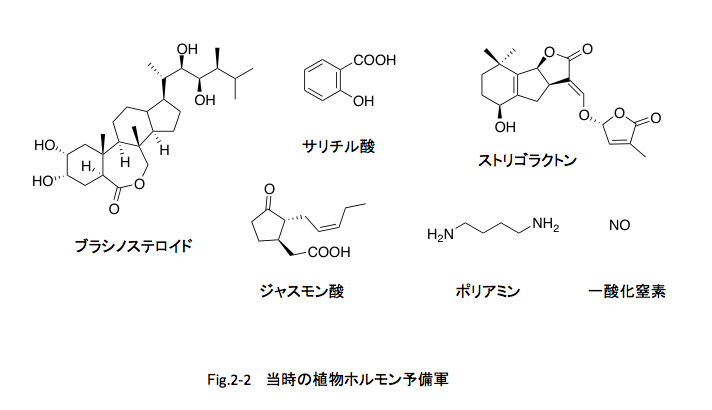

例外はRNAであるフロリゲンである。また、1999年にC. A. Gehringがナトリウム利尿ペプチドの一種が植物のホルモンではないかという報告を書いているし、その後20種近いペプチドが植物ホルモン候補として報告されているが、現在のところまだ認知されてはいないようである。では動物ホルモン群と植物ホルモンの物質群の大きな違いは何に起因するのか?答えは、まだない。
もう一つの疑問は『何故アブシジン酸は植物ホルモンであるのか?』という疑問である。振り出しに戻っただけではないかと言われそうだが、そうではない。「アブシジン酸の分子構造は、何故アブシジン酸の作用をもたらすのか」という疑問に進化しているのである。ホルモンの定義は「特定の分泌腺で生合成され、血液やリンパ液で標的臓器に運ばれ、そこで特異的な生理過程に影響を与える微量物質」である。この定義は生理学的側面からの定義であって、その中にはホルモン分子の構造に関する概念が全く含まれていないと思っていた。だが、この定義を現代風に書き換えるとすれば、「特定の分泌腺で生合成され、血液やリンパ液で標的臓器に運ばれ、標的臓器において当該ホルモン作用を発現するカスケード系の始点にあるレセプタータンパク質に特異的に結合する物質をいう」とでもなるだろう。とすれば、レセプタータンパク質に特異的に結合できる物質は、特異的な構造を持たねばならない。我田引水・牽強付会的な無理のある解釈だが、古典的な定義の中に構造を指定する概念があったともいえる。
この前提に立てば、アブシジン酸はアブシジン酸レセプターに結合できる構造を持つ。従ってアブシジン酸はアブシジン酸の活性を示すというのが結論となる。当たり前すぎる結論で馬鹿馬鹿しくなってきた。あれ、アブシジン酸と結合するレセプターをアブシジン酸レセプターという。いやいや、私の単純な頭ではわからなくなってきた。抗原と抗体の場合と同じく、相互に依存した循環定義になってしまったようだ。それにしても、レセプターを介してホルモンを定義しようとすると、さらに厄介な問題が起こってくる。レセプターは進化するのである。
さて、酵素タンパク質、構造タンパク質あるいはレセプターと呼ばれるタンパク質が、ある原始的なタンパク質に由来し、種々の変異を繰り返しながら、いわゆるファミリーという概念で分類されるタンパク質群を形成してきたことはよく知られている。荒っぽい議論だが、機能を獲得したタンパク質分子は、遺伝子の変異・重複、サイズの拡大・縮小、あるいは転移などを通して進化する。ではこの進化するレセプタータンパク質と相互作用するリガンド分子が進化することはないのであろうか。
ペプチド性リガンド(タンパク質リガンドを含む)が進化することは、レセプター分子の場合と同様自明のことであろう。ヒトのインシュリンとチンパンジー、イヌ、ネコのインスリンは、110個のアミノ酸配列の中でそれぞれ2カ所、13カ所、21カ所のアミノ酸残基が異なっている。この事実に対して違和感を感じている研究者に出会ったことはない。彼らの意識の中で、ペプチド性リガンド分子は進化(変化)しても当たり前なのである。
では低分子リガンドの場合は、どう考えればいいのだろうか。例えば、ステロイドレセプターはアロステリックタンパクである。このタンパク質は、ホルモン分子との結合部位とDNA との結合部位を持ち、ホルモン分子が結合すると、DNAとの結合部位の形が変化する。この変化を通して、レセプター分子とDNAとの結合能力が制御されている。このレセプター分子において、変異がホルモン分子との結合部位に起こればホルモン分子との親和性あるいはホルモン分子に対する選択制に変化が起こるであろうし、 DNA との結合部位に起こればDNA との結合能あるいは結合場所に変化が起こることになる。
こうした変異すなわち進化が重なって、ステロイドホルモンレセプターは、ファミリーあるいはスーパーファミリーと呼ばれるレセプター群を形成している。そしてこのスーパーファミリーには、いわゆるステロイド骨格を持つ性ホルモン(エストラジオール、テストステロン、エストロンなど)、副腎皮質ホルモンレセプター(コルチゾール、アルドステロンなど)、昆虫の脱皮ホルモン(エクダイソン、エクジステロン)のレセプター群だけでなく、ステロイド骨格を持たない、レチノイン酸、チロキシン、ビタミンD3、あるいはプロスタグランジンのレセプター群も含まれている。ということは、こうした異なった生合成系を持つ全くまとまりのないリガンド群について、それらの化合物の間に何らかの類似性の存在を担保しなければならない。では何が類似性を担保するかといえば、それは構造である。レセプターの進化に伴いリガンドとの結合部位が変化することを考慮すれば、リガンドも変化(進化)することを認めざるを得ないと考えるのだが、低分子リガンドの進化という表現をすると、何故か頭から否定される場合が多い。どうやら、進化という概念は化学物質には適用できないと考えている方が多いようだ。
ところで、近年は分子生物学全盛の時代である。若者に危険・臭い・汚い・きついというイメージを持たれてしまった、4K有機化学の人気は低迷を続けている。しかしながら、生物体内で起こっている代謝は、すべて有機化学反応である。例えば、分子生物学的研究を進めるに際して汎用される○○キットと呼ばれる製品群は非常に便利で結果を簡便に与えるように作ってあり、一寸した遺伝子組み換え程度なら高校生にもできるようになった。こうしたキットにおいては、プロトコル(使用に際してのマニュアル)は充実しているが、キットで起こっている現象の作動原理を明示していないものが多い。そしてかなり多くの研究者と呼ばれる人々が、このブラックボックスを内包したキットに依存して研究をおこなう、キット依存症候群を発症している。
例えば、DNAの複製、転写、逆転写、つまりPCR法で使われている反応群は、2分子求核置換反応(SN2反応)に分類される壮大なリン酸エステルの合成である。タンパク質合成においては、アミノ酸をtRNAに結合させる反応が混合酸無水物法に分類されるエステル化反応であり、リボソームおける翻訳段階が、これまた活性エステル化法に基ずく膨大なアミド結合の合成であることに気づいていない研究者が、世の中には多数生息しているのである。
なぜこんな話をするかといえば、有機化学を思考の基盤とする人間からみると、理解に苦しむような場面に良く出会うからである。例えば、ステロイドホルモンレセプター群と称される一群のレセプタータンパク質がある。このレセプター群の個々のレセプターは、それぞれが対応するリガンドを持っているのだが、有機化学者の目から見るとリガンド群の化合物としての構成におおきな違和感が存在する。
遺伝子を通して生物を見ている研究者たちは、生物の理解において非常に有益な情報を提供してくれる。これは間違いのない事実である。彼らはしかし、扱う対象が構成要素は単純であるにしても巨大な分子であるため、対象を分子式・構造式としてみるのではなく、単なる名称あるいは簡素化した記号としてみる習性を身につけてしまったようだ。有機化学者の立場からみると、ステロイド(ビタミンD3?)、レチノイン酸、チロキシン、プロスタグランジンは、それぞれ大きく異なった化合物群に属しているからである。(図2-3)
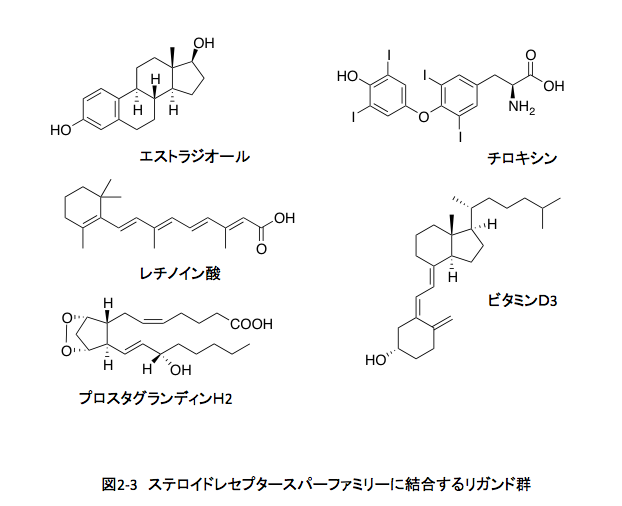

生合成から見ても化合物の形から見ても、これらが同じファミリーに属するレセプター群に結合するとは考えにくい。しかし、現実にはこれらの異質な化合物群が一連のレセプター群のリガンドとして機能している。なぜか?
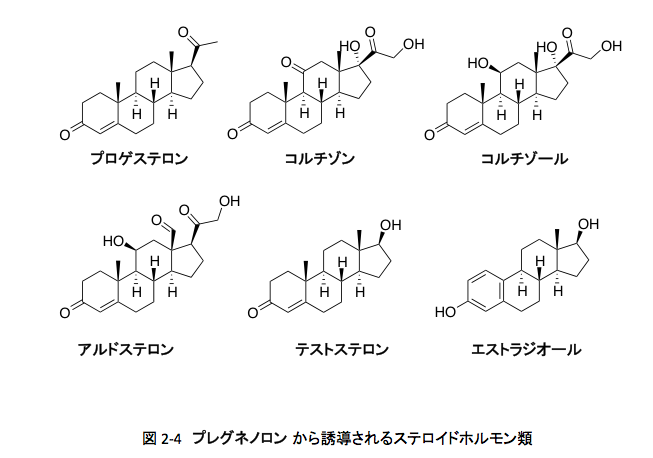
レセプターは進化に伴って変化する。それは当然のことだとしても、変化の程度には大きな差があるに違いない。レセプターをコードするDNA塩基配列の1カ所に突然変異が起こり、この変異に伴いアミノ酸1残基が変化したとする。これは最も小さな変異であると考えてよい。しかし、たった1アミノ酸残基の変化であっても、変化の起こる位置と変化した後のアミノ酸の種類によっては、レセプターの変異の性質は大きく異なって来る。レセプターの小さな変化は、同じ生合成系に属し少しずつ構造が異なっているリガンド群、例えばプレグネノロンを中間体として生合成されるステロイドホルモン類-プロゲステロン、コルチゾン、コルチゾール、アルドステロン、テストステロン、エストラジオールなどに対応するだろう。

一方、リガンドの結合部位の大きな変化は、構造上大きな違いを持つリガンド群であるステロイド(イソプレノイド:C30のスクアレンからC9~C12を含む炭素鎖を切り捨てたもの)、レチノイン酸(イソプレノイド:C40のヨノン環を一つ切り捨て、さらにC10単位の炭素鎖を切り捨てたもの)、チロキシン(シキミ酸系化合物:アミノ酸であるチロシンの3,5位がヨウ素化された後、酸化的にカップリングしたもの)、プロスタグランジン(ポリケチド:脂肪酸合成系を通りアラキドン酸まで不飽和化が進行した後、プロスタグランジンエンドペルオキシドシンターゼによる1,2-ジオキサシクロペンタンとシクロペンタンの縮合環形成に続くプロスタグランジン類とトロンボキサン生合成系で生合成されたもの)など、構造だけではなく生合成から見て違うカテゴリーに属する化合物が、リガンドとして機能しはじめたこと対応すると考えられるのではないか。
こうした大きな変異がレセプターで起こった場合には、いままでリガンドではなかった全く異質な分子であっても、その一部の構造がレセプターに結合できる程度に似てさえいれば、リガンドとして機能し始める可能性を持つに違いない。だが、こんなことを言うと、その化合物が働くのに適切な濃度の制御、つまり生合成速度と分解速度の調節などがそんなにうまくいくのかという問題をすぐに提起される。しかしながら、この問題は、最初のリガンドが働き始めた場合であっても当然存在した問題であり、生理学的有効濃度をうまく維持するメカニズムを持っていた生物が生き延びたと考えるしかない。この話の最後の部分は、前適応という考え方を借りた形になっている。前適応という概念は、本音のところではあまり好きではない。生物の形質レベルでこの概念を使うことには、いくぶん以上の違和感を持っている。しかし、リガンドの乗換、言い換えると新規なリガンドによるレセプターの乗っ取りに関しては、十分な蓋然性があると考えている。理由については、後で述べる「Oxygenic burst仮説」において詳述することにする。
話がアブシジン酸から離れてしまったように見えるかもしれないが、実はアブシジン酸の由来の話をしているのである。アブシジン酸も、生物の長い歴史の中でいわゆるホルモン活性を獲得した分子であると考えなければならない。歴史上のある時点で、植物がたまたま作り出したレセプタータンパク質に対し、構造的親和性を持つ分子であるアブシジン酸が出現し、ある機能をはたし始めたのである。たまたま作り出されたレセプタータンパク質とアブシジン酸の歴史はどちらが長いのか?それはまだ分からないが、アブシジン酸の方が古ければ、アブシジン酸分子が前適応という形で存在していたと言う話になるであろうし、レセプタータンパク質の方が古ければ、レセプタータンパク質が前適応で説明されるオーファンレセプターであったということになる。私はレセプターの歴史の方が長いと考えている。理由は後述する。
議論が錯綜してきたが、要するにアブシジン酸に限らず植物ホルモンと呼ばれる化合物群(或いはホルモンと呼ばれる全ての化合物群)については、解決されていない多くの疑問が残っているのである。この部分をブラックボックスとして研究を進めることは可能だが、私はそれらの疑問に拘泥しており、なかなか応用的研究には進む気にはなれない。では私は何をすればよいのか。多くの論文を読んでわかったことは、有機化学を指向する研究者は高活性の化合物を求めて精密かつ効率的なな有機合成の道を走り、生理学を指向する研究者はアブシジン酸の生合成系の解明や生理現象の解析に走り、分析化学を指向する研究者は植物中の内生量の検討やケモタクソノミー(化学分類学)などを目指して進んでいる。しかし、アブシジン酸とは本来何者であるかという発想で研究している人はいない。
ここに私の居場所があると感じた。私は、一応有機化学に片足を乗せた研究者である。有機化学を基礎とする研究者としてアブシジン酸に向き合うに際し、アブシジン酸を自明のホルモンとして認めるのではなく、アブシジン酸の分子構造をアンカーとし、そこから分布、生合成、生理活性などについて総合的に考えようと思ったのである。このタイプの発想は、ある分野の大家が退官を前にして持つものであり、おまえみたいな若造がという批判はあった。そんな発想では「実験ができないだけでなく報告も書けないよ」とする親切かつ正しいアドバイスもあった。思い上がりであったかも知れないが、そうした反応があることはわかった上でのテーマ設定であり、本人としては科学哲学分野への転身かもしれないと考えていた。